Diagnose
Pseudoxanthoma elasticum (PXE)
THERAPIE UND VERLAUF
Da PXE eine systemische Erkrankung ist, wurde unsere Patientin zur kardiologischen und ophthalmologischen Untersuchung überwiesen, um eine Beteiligung des Herzens und der Augen auszuschließen. Die Patientin und ihre Verwandten wurden über die genetischen Ursachen der Erkrankung informiert. Um die entzündlichen Papeln am Hals und in den Achselhöhlen zu lindern, begannen wir eine kurzzeitige topische Behandlung mit einer Steroidsalbe der Klasse III (Methylprednisolonaceponat) in Kombination mit Chlorhexidin.
DISKUSSION
Pseudoxanthoma elasticum ist eine seltene, autosomal rezessiv vererbte systemische Stoffwechselerkrankung des elastischen Bindegewebes, die typischerweise die Haut, die Netzhaut und die Blutgefäße befällt (Prävalenz 1 : 25.000, OMIM264800). (1) Darier, der Erstbeschreiber der Erkrankung, gab ihr 1896 den Namen Pseudoxanthoma elasticum. (2) Pseudoxanthoma elasticum wird durch Mutationen im ABCC6-Gen (ATP binding cassette subtype C number 6) verursacht, das für die Familie der ATP-abhängigen Transmembrantransporter (auch MRP6 genannt) kodiert.
Das ABCC6-Gen ist von grundlegender Bedeutung für die Regulation der Mineralisierung durch Kontrolle der ATP-Freisetzung. Nonsense-, Missense-, Frameshift- oder große Mutationen führen zu einer veränderten Produktion von Pyrophosphat, einem ATP-Derivat, das die ektopische Mineralisation steuert. Bei homozygoten Mutationsträgern führt dies zu dystrophischer Verkalkung elastischer Fasern durch abnorme Anhäufung von Kalzium- und Phosphationen. (3)
Die wichtigsten Hautmanifestationen sind gelbliche Papeln, vor allem in den Beugebereichen einschließlich der seitlichen Halsregion, der periumbilikalen Region, der Leistengegend und der Kniekehle. Diese Läsionen neigen dazu, zu konfluieren und netzartige Plaques zu bilden, die sich auf die nichtbeugenden Bereiche ausdehnen. (4) Im weiteren Verlauf entwickeln sich die Plaques zu einem kopfsteinpflasterartigen Hautbild, wie es bei unserer Patientin beobachtet wurde (Abbildung 1). Auch die innere Unterlippe sowie die Vaginal- und Rektalschleimhaut können betroffen sein. Die Hautveränderungen müssen von anderen hereditären und erworbenen elastolytischen Erkrankungen abgegrenzt werden (zum Beispiel mitteldermale Elastolyse, solare Elastose, Pseusoxanthoma-elasticum-ähnliche papilläre dermale Elastolyse, weiße fibröse Papulose des Halses). Eine umfassende Liste von Differenzialdiagnosen wurde publiziert. (5)
Ärzte müssen sich des systemischen Charakters der Erkrankung bewusst sein und eine interdisziplinäre Beurteilung von PXE-Patienten zusammen mit Augenärzten und Kardiologen einleiten. Zwei sehr häufige und normalerweise symptomlose ophthalmologische Anzeichen für eine Augenbeteiligung sind das „Kometenzeichen“ (ein einzelner weißer Körper mit einem weißen Schwanz aus atrophischem retinalem Pigmentepithel) und retinale Peau-d’Orange-Veränderungen. Die ersten weißschwänzigen Flecken befinden sich in der Peripherie der Netzhaut, eine Sprenkelung des Netzhautepithels. In höherem Alter können PXE-Patienten Risse entlang der Bruchschen Membran entwickeln, die auch die Makula betreffen können, die sogenannten angioiden Streifen (AS). (6) Im Laufe der Jahre kann es bei diesen Patienten zu Metamorphopsie oder zentralem Sehverlust aufgrund von Netzhautblutungen kommen. Die Gefäßbeteiligung ist auf dystrophische Verkalkungen zurückzuführen, die in der Media und Intima der Blutgefäße (meist kleine und mittelgroße Arterien) auftreten. (7) Diese Veränderungen können zu Claudicatio intermittens, peripherem Pulsverlust, renovaskulärer Hypertonie, Angina pectoris, Schlaganfall, transitorischer ischämischer Attacke, Verengung der Radial- oder Karotisarterien oder sogar der Aorta führen. In seltenen und schwersten Fällen wurden Myokardinfarkte beschrieben, die zum frühen Tod der Patienten führten. (8–10)
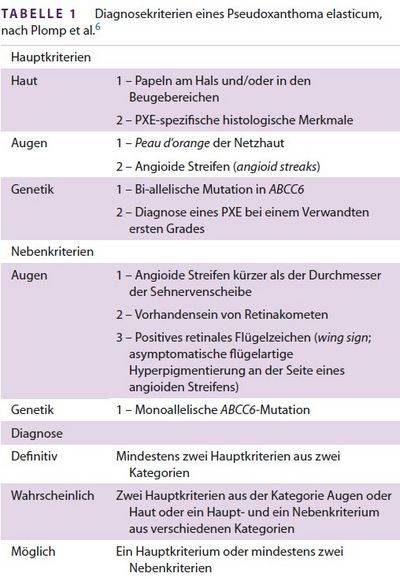
Die Diagnose von PXE ist schwierig und basiert auf Haupt- und Nebenkriterien aus den Kategorien (1) kutane Veränderungen, (2) ophthalmologische Veränderungen, (3) genetische Veränderungen. (6) Wegen Pseudogenen (nichtkodierende Sequenzen mit Ähnlichkeit zur Protein-kodierenden Sequenz) kann die molekulare Diagnose eine große Herausforderung darstellen. (6) Anhand dieser Kriterien wird das Vorhandensein von PXE in „definitive“, „wahrscheinliche“ oder „mögliche“ PXE eingeteilt (Tabelle 1). (6) Nach dieser Klassifizierung wurde bei unserer Patientin eine wahrscheinliche PXE-Diagnose gestellt, da eine Netzhautbeteiligung ausgeschlossen wurde und die Patientin einer genetischen Analyse nicht zustimmte. Die Behandlung der Hautläsionen ist schwierig. Die chirurgische Entfernung oder die Entfernung mit einem CO2-Laser ist eine Möglichkeit, aber die Läsionen neigen zum Rezidiv. Einige Autoren vermuten, dass die orale Gabe von Magnesium die PXE-induzierte Verkalkung verhindern
oder abmildern kann. Kürzlich führte die Verabreichung von Minocyclin in einem Zebrafisch ABCC–/–-Modell zu verringerter Mineralisierung und Verkalkung, was auf einen möglichen Ansatz für künftige Versuche am Menschen hinweist. (11)
DANKSAGUNG
Die Patientin in diesem Manuskript hat schriftlich ihr Einverständnis zur Veröffentlichung ihrer Falldetails gegeben. Dr. med. Farzan Solimani ist Teilnehmer des BIH Charité Clinician Scientist Program, das von der Charité – Universitätsmedizin Berlin und dem Berliner Institut für Gesundheit der Charité (BIH) finanziert wird.
Interessenkonflikt
Keiner.
LITERATUR
1. Tronnier M. Cutaneous disorders characterized by elastolysis or loss of elastic tissue. J Dtsch Dermatol Ges. 2018;16:183-191.
2. Darier J. Pseudoxanthoma Elasticum. Monatshefte für Praktische Dermatologie. 1896;23:609-617.
3. Chassaing N, Martin L, Calvas P, et al. Pseudoxanthoma elasticum: A clinical, pathophysiological and genetic update including 11 novel ABCC6 mutations. JMedGenet. 2005;42:881-892.
4. Marconi B, Bobyr I, Campanati A, et al. Pseudoxanthoma elasticum and skin: Clinical manifestations, histopathology, pathomechanism, perspectives of treatment. Intractable Rare Dis Res. 2015;4:113- 122.
5. larusso J, Li Q, Uitto J. Pseudoxanthoma elasticum, the paradigm of heritable ectopic mineralization disorders – can diet help? J Dtsch Dermatol Ges. 2011;9:586-593.
6. Plomp AS, Toonstra J, Bergen AA, et al. Proposal for updating the pseudoxanthoma elasticum classification system and a review of the clinical findings. Am JMed Genet A. 2010;152A:1049-1058.
7. Leftheriotis G, Omarjee L, Le Saux O, et al. The vascular phenotype in Pseudoxanthoma elasticum and related disorders: Contribution of a genetic disease to the understanding of vascular calcification. Front Genet. 2013;4:4.
8. Boutouyrie P, Germain DP, Tropeano AI, et al. Compressibility of the carotid artery in patients with pseudoxanthoma elasticum. Hypertension. 2001;38:1181-1184.
9. van den Berg JS, Hennekam RC, Cruysberg JR, et al. Prevalence of symptomatic intracranial aneurysmand ischaemic stroke in pseudoxanthoma elasticum. Cerebrovasc Dis. 2000;10:315-319.
10. Vasseur M, Carsin-Nicol B, Ebran JM, et al. Carotid rete mirabile and pseudoxanthoma elasticum: an accidental association? Eur J Vasc Endovasc Surg. 2011;42:292-294.
11. Nollet L, Van Gils M, Willaert A, et al. Minocycline attenuates excessive DNA damage response and reduces ectopic calcification in Pseudoxanthoma elasticum. J Invest Dermatol. 2022;142:1629- 1638e6.

Die Diagnosequizze werden uns freundlicherweise zur Verfügung gestellt vom
"Journal der Deutschen Dermatologischen Gesellschaft" © Deutsche Dermatologische Gesellschaft
![Logo: Junge Dermatologen im Berufsverband der deutschen Dermatologen - zur Startseite [ALT+1]](/typo3conf/ext/judermconfig/Resources/Public/Images/Branding/JuDermLogo.png?v=2)